|
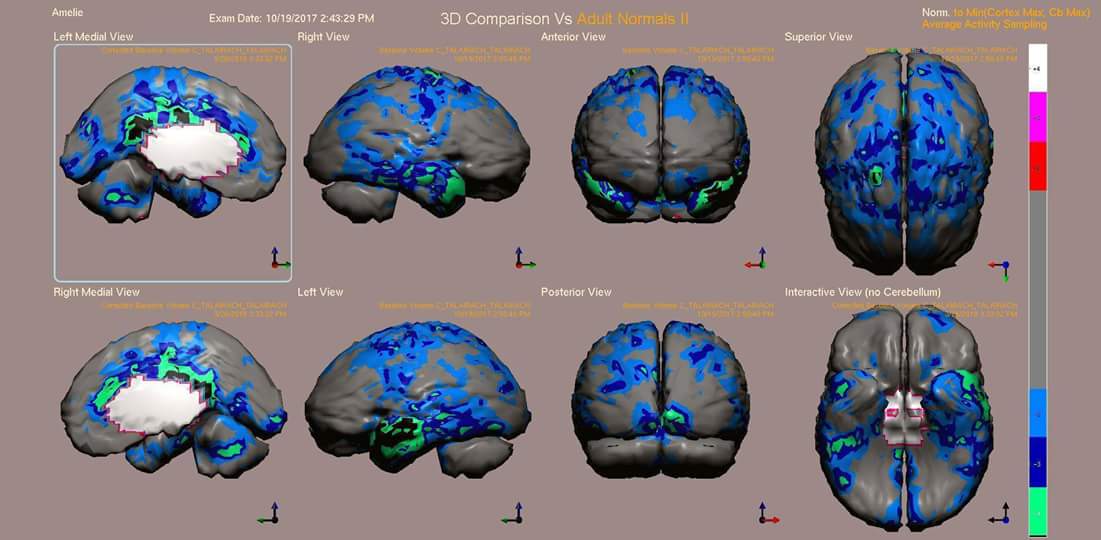
Comme plusieurs autres maladies du système immunitaire, la plainte la plus fréquente exprimée par les patients atteints de SAMA serait la « fatigue ». Voici d'ailleurs les termes que le Dr. Lawrence Afrin utilise pour décrire la fatigue de sa patiente à la page 1 de son livre « Never Bet Against Occam: Mast Cell Activation Disease and the Modern Epidemics of Chronic Illness and Medical Complexity »: « Elle était fatiguée. Quand je suis entré dans la salle d'examen, le tout premier jour où j'ai rencontré ma « patiente #1 » en mars 2008, sa fatigue marquée était évidente, presque palpable. Elle avait d'autres problèmes de santé également, plusieurs en fait! Mais la « fatigue » était sa « plainte principale », pour utiliser la terminologie professionnelle sous-entendant un patient « plaignard ». Elle avait réussi à se rendre à la clinique, puis marcher jusqu'à la salle d'examen par elle-même, sans utiliser d'aide technique pour se mobiliser, mais son type de fatigue n'avait rien à voir avec un épuisement normal suite à l'effort. Et cette fatigue avait encore moins à voir avec le genre de fatigue que les gens vivent à cause d'un manque de sommeil. Non, c'était le genre d'épuisement pour lequel le terme « malaise » a été inventé. Un manque total d'énergie, et ce, pour aucune raison apparente. À peine âgée de 58 ans, sa vie avait été ruinée par cette fatigue drainante. Auparavant une femme d'affaire indépendante dont la carrière était couronnée de succès, remplie d'énergie, athlétique, intelligente, et hautement productive; à cause de cette fatigue progressive, qui avait empirée au cours des années, elle n'était maintenant plus que l'ombre d'elle-même. Elle n'était même plus capable de monter un seul escalier dans son domicile, et encore moins de continuer à aller faire du jogging à tous les jours comme elle avait apprécié le faire pendant des décennies. Entièrement épuisée, elle avait dû fermer sa compagnie. Et les traitements qu'elle recevait pour la maladie qu'on lui avait diagnostiquée semblait empirer sa situation. » Si cette description vous fait penser à une autre entité clinique, soit le « syndrome de fatigue chronique », moi aussi. À noter que, par conviction personnelle, je n'inclue pas ici l'encéphalomyélite myalgique dans cette définition, bien qu'au Québec, et ailleurs dans le monde, les deux noms soient utilisés ensemble, de façon interchangeable. Or, cela peut malheureusement s'avérer problématique, à divers niveau, lorsqu'on observe plus attentivement l'origine de ces termes. De 2012 à 2019, j'ai eu la chance, et le privilège, d'être suivie par le Dr. Byron Hyde de la Fondation Nightingale pour la recherche. Depuis 1984 (donc, avant que l’encéphalomyélite myalgique ne soit renommée « syndrome de fatigue chronique »), le Dr. Hyde a consacré sa carrière à l'investigation de patients qui ont reçu un diagnostic d'encéphalomyélite myalgique et/ou de syndrome de fatigue chronique, fibromyalgie, et autres syndromes de fatigue post-virale. Selon ses recherches et son expérience clinique, l'encéphalomyélite myalgique serait aujourd'hui très proche de ce qu'on appelait, avant 1955, la « poliomyélite atypique ». Le terme « encéphalomyélite myalgique bénigne » a d’ailleurs été utilisé pour la première fois cette année-là, afin de décrire une épidémie « similaire à la polio » qui a touché 292 employés (infirmières, médecins, personnel administratif…) et 12 patients du « Royal Free Hospital », à Londres. Ces événements sont survenus la même année où une épidémie de poliomyélite paralytique et atypique frappait Londres et le reste de l’Angleterre. D'un point de vue éthymologique, le terme « encéphalomyélite myalgique » signifie « inflammation du cerveau et de la moelle épinière, accompagnée de douleurs musculaires ». On l’appelait alors « bénigne », puisqu’elle ne causait généralement pas de décès et/ou de paralysie flasque, contrairement à la poliomyélite (quoiqu’il existe quand même certains rares cas d’EM qui ont développé de la paralysie, ou bien sont décédés des suites de l’évolution de la maladie). Puis, quelques années plus tard, le Dr. Ramsey a suggéré que le terme « bénin » soit retiré de son appellation, pour mieux refléter la sévérité et l’impact significatif de la maladie sur le patient. La phase initiale prenait la forme soit d’une infection des voies respiratoires supérieures avec un mal de gorge, une irritation oculaire, et de la toux sèche; ou bien de troubles gastro-intestinaux avec de la nausée, de la diarrhée, et des crampes. La lassitude générale, les maux de tête, la douleur musculaire, le vertige et les étourdissements étaient, quant à eux, des symptômes quasi toujours présents dans les 2 cas. L’infection pouvait être accompagnée de faible élévation de température corporelle qui s’élevait rarement à plus de 38 degrés Celsius. La plupart du temps, les glandes cervicales postérieures étaient élargies et sensibles, et les patients ressentaient de la douleur au bas de la nuque. Quelques cas ont souffert de paralysie (dont au moins un cas où celle-ci aura duré plus de 60 ans). Outre les trois entérovirus reconnus comme pouvant causer la polio, et contre lesquels les vaccins Salk et Sabin se sont avérés si efficaces que les cas de décès et de paralysie flasque sont disparus presqu'instantanément, il existe au moins une centaine d'autres entérovirus de la même classe pouvant également causer des symptômes sévères et invalidants (dont certains cas plus isolés de paralysie flasque et de décès), et dont la structure génétique présente, chez certains, moins de 5% de différence avec les trois poliovirus reconnus. Malheureusement, bien que les médecins ayant investigué ces patients en 1955 en étaient venus à la conclusion qu'il s'agissait d'une épidémie d'origine entérovirale; en 1970, des psychiatres britaniques se sont à nouveau penché sur la cause probable de ces événement. Ils en sont venus à la conclusion qu'une « hystérie de masse », et non un virus, aurait plutôt été à la source de la maladie du Royal Free, comparant celle-ci au « syndrome de respiration exagérée » observé chez de jeunes fillettes d'âge scolaire. L'argument de taille, qui fut utilisé pour appuyer leur théorie, était que la maladie affectait principalement les femmes*. Ce qui aurait pu être investi comme temps, efforts, ressources, et argent, dans la recherche médicale de maladies d'origine virale probables, survenues à peu près au même moment, telles que la maladie du Royal Free, la neuromyasthénie épidémique, et la maladie d’Akureyri, fut donc plutôt réorienté vers l'approche psychologique et béhavioriste. [*En 2021, il est intéressant de noter que, bien qu'on semble rapporter un plus haut taux de mortalité chez les hommes atteints du COVID; les patients qui développent la forme chronique de la maladie (le fameux « COVID long »), dont les symptômes rapportés s'apparentent énormément à l'encéphalomyélite myalgique, sont toujours majoritairement des femmes.] Puis, en 1984, est survenue une autre pandémie mondiale de cas d’encéphalomyélite myalgique qui, en Amérique du Nord, a touché particulièrement le Lac Tahoe au Nevada, la Caroline du Nord, Montréal, et plusieurs régions de l’Ontario. Dans 20 cas d’infection investigués par Dr. Hyde à l’époque, des virus de la même classe que les poliovirus ont été également retrouvés. Il s’agit d’entérovirus Coxsackie, Echo, et similaires à Echo-21. Par contre, les médecins de l’époque ont plutôt cru que le virus de la mononucléose (Epstein-Barr, souvent désigné par l'acronyme EBV) était la source du problème, et se sont mis à appeler la maladie « syndrome du virus d’Epstein-Barr chronique ». Cette théorie fut rapidement démentie et, en 1988, les Centres pour le contrôle et la prévention des maladies ont proposé l’appellation « syndrome de fatigue chronique » en remplacement. Malheureusement, au lieu de stimuler la recherche et d’encourager le financement d’autres études visant à explorer l’aspect épidémiologique et physiopathologique de la maladie, ce changement de nom semble plutôt avoir eu pour effet de banaliser l’encéphalomyélite myalgique. Plusieurs des particularités cliniques de la maladie, pourtant jusque-là bien documentées, ont été oubliées et/ou mises de côté pour rendre la définition clinique moins restrictive, augmentant ainsi le risque de poser le mauvais diagnostic en incluant trop de patients souffrant de pathologies différentes à l’intérieur de la même définition. Ce diagnostic s'est un peu transformé en une constellation de signes et symptômes pouvant appartenir à des centaines de maladies différentes, dont plusieurs très invalidantes et sévères; mais dont aucune manifestation clinique n'est exclusivement spécifique à l'une d'entre elles. Chez les patients que Dr. Hyde investigue, celui-ci affirme pouvoir généralement trouver la ou les causes sous-jacentes derrière les symptômes du patient dans 70% à 80% des cas. Les diagnostics jusque-là non-décelés qu’il a pu identifier chez ces personnes diagnostiquées « EM/SFC » incluent, entres autres : encéphalopathie diabétique, obstruction partielle des artères carotides et obstruction totale de l’artère basilaire, cancer de la thyroïde, cancer de la prostate, syndrome de Gougerot-Sjögren, réaction adverse à la pilule anticonceptionnelle, parasites intestinaux, épilepsie nocturne avec bloc cardiaque entraînant une syncope, et syndrome d’Arnold-Chiari avec ventriculomégalie cérébrale. Parmi huit échantillons, prélevés sur des patients avec un diagnostic d’EM/SFC qui avaient été envoyés au même moment afin d’être analysés pour vérifier la présence d’infection antérieure par entérovirus en 2012, je faisais partie des 2 résultats qui étaient revenus entièrement négatifs. Une des difficultés rencontrées chez moi, du point de vue des inverstigations médicales avec Dr. Hyde, était qu’on réussissait souvent à trouver quelques petites anomalies au niveau de mes résultats de tests et d'analyses, ainsi qu’à travers mes manifestations cliniques, mais celles-ci ne cadraient jamais tout à fait parfaitement avec une pathologie déjà connue. Ma fatigue, par contre, était définitivement très typique des patients diagnostiqués EM/SFC. Éventuellement, il m'a fait passer une scintigraphie cérébrale avec HMPAO. Les résultats se sont avérés être très typiques de ses patients atteints d'encéphalomyélite myalgique suite à une infection entérovirale. Légende - Zone grise: Perfusion sanguine normale - Zone bleu pâle: Atteinte vasculaire / hypoperfusion 2 écarts-type sous la normale. - Zone bleu foncée: Atteinte vasculaire / hypoperfusion 3 écarts-type sous la normale. - Zone verte: Atteinte vasculaire / hypoperfusion 4 écarts-type sous la normale. - Zone noire: Hypoxie / absence de circulation. 
Dans mon cas, l'élément déclencheur majeur identifié était la mononucléose, mais d'autres facteurs suggèrent que je souffrais déjà probablement d'une certaine dysfonction au niveau du fonctionnement de mes mastocytes avant cet événement. Et c'est ici que, plus j'en apprends sur ces différents syndromes, et plus je commence à vivre un certain dilemme concernant ce qui appartient à l'un, vs à l'autre. Puisque le SAMA est un trouble de santé impliquant un processus inflammatoire qui peut traverser la barrière hémato-encéphalique et causer de l'inflammation cérébrale, est-ce que cette inflammation cérébrale pourrait en venir à aller affecter de façon similaire les mêmes zones cérébrales impliquées dans ce que Dr. Hyde a pu observer chez ses patients ayant développé l'EM suite à une infection d'origine entérovirale?Ce ne sont pas tous les patients atteints de SAMA dont les manifestations cadrent également dans la définition clinique de l'EM, et ou de L'EM/SFC du Concensus Canadien (qui est différent de la définition utilisée par Dr. Hyde pour l'EM, plus spécifiquement), non plus. Et ce n'est pas tous les cas d'EM ou bien d'EM/SFC qui souffrent des manifestations pseudo-allergiques plus franches qu'on tend à retrouver dans le SAMA. Mon impression personnelle, est que ce qu'on décrit dans l'EM/SFC (selon la définition du Concensus Canadien) est probablement un ensemble de plusieurs syndromes qui se déclarent suite à plusieurs facteurs déclencheurs différents (infections virales, dysfonctions du système immunitaire, maladies mitochondriales, traumatismes crâniens, etc.) et finissent par aller causer le type de fatigue invalidante, non soulagée par le repos, et exacerbée à l'effort, qu'on retrouve chez ces patients. Et le fait que Dr. Hyde ait isolé, de façon plus spécifique, une cohorte de patients qui ont tous été mis en contact avec un entérovirus similaire à la poliomyélite, pourrait probablement jouer un rôle significatif dans la prise en charge précoce et le traitement, mais aussi dans la prévention de telles infections. Présentement, nous semblons voir éclore un autre sous-groupe de patients avec des manifestations cliniques similaires, mais causées plus spécifiquement par le virus du COVID. Certains patients n'avaient aucun trouble neurocognitif, ni de problèmes d'asthme, d'eczéma, ou d'allergies avant de développer l'EM/SFC. D'autres oui. Donc, pour en revenir plus spécifiquement au symptôme de la fatigue, je m'interroge un peu sur la possiblité que ce type de fatigue puisse ne pas être absolument exclusive et unique à l'EM/SFC en tant que tel. Je sais qu'il est généralement accepté par la communauté scientifique, et même par plusieurs groupes de patients, que l'augmentation graduelle du niveau d'activité physique chez les patients atteints de lupus, de fibromyalgie, ou de la maladie de Crohn, en suivant un modèle d'exercices gradués, ne risque pas d’avoir un impact négatif sur leurs capacités fonctionnelles, mais plutôt venir leur offrir un soulagement de leurs symptômes de fatigue et les aider à améliorer leurs capacités. Or voilà, si on prend bien le temps d'interagir avec des membres de ces autres communautés de patients, on s'aperçoit rapidement qu'un bon sous-groupe de ceux-ci décrivent le même malaise après l'effort qu'on retrouve dans l'EM/SFC (en utilisant une terminologie différente), accompagné souvent d'un temps de récupération anormalement long. Ces patients apprendront alors l'approche du « pacing » (i.e. alterner périodes d’activités avec périodes de repos), et de la gestion de leurs activités quotidiennes en fonction de leur énergie journalière disponible. Comme on utilise souvent des « cuillères » (en anglais, « spoons ») pour symboliser chaque unité d'énergie disponible pour effecter les tâches journalières, certains patients atteints de ces maladies chroniques vont se donner comme surnom les « spoonies ». Et, bien que la plupart des recherches cliniques vont démontrer que les patients atteints de différentes maladies immunitaires et auto-immunes vont améliorer leurs capacités fonctionnelles et leur endurance musculaire grâce à des programmes d’exercice où on augmente graduellement l’effort à fournir; il y a certains sous-groupes de ces populations de patients qui « n’arrivent pas à se discipliner », et qui « refusent de collaborer avec leur médecin et leurs thérapeutes en acceptant d’effectuer les efforts nécessaires pour atteindre les objectifs raisonnables et sécuritaires de leur programme de réadaptation ». Il y a de ces patients, atteints de colite ulcéreuse par exemple, qui « semblent souffrir d’une phobie de l’activité physique, et/ou entretiennent des inquiétudes exagérées, persistantes et envahissantes en lien avec l’impact négatif que pourrait avoir l’activité physique sur leur état de santé ». En résumé, si la grande majorité des patients souffrant de la même maladie répondent bien à la thérapie par exercices gradués, n’éprouvent pas de malaise significatif suite à l’effort, ont une période de récupération raisonnable, et ne voient pas leurs autres symptômes s’empirer de façon significative des suites de l’exercice; il semble raisonnable d'assumer que les quelques patients qui, eux, affirment avoir une réaction adverse à l’activité physique, souffriraient plutôt d’un trouble anxieux, dépressif, ou bien manqueraient de volonté et de discipline. S’ils rencontrent un médecin familier avec l’EM/SFC, certains de ces patients atteints de maladies chroniques, qui sont particulièrement intolérants à l'activité physique, se verront possiblement également offrir un diagnostic d'EM/SFC en plus de celui de leur autre maladie. Une personne pourra donc être atteinte à la fois du lupus systémique, et diagnostiquée EM/SFC. De fibromyalgie et d'EM/SFC, etc. On attribuera donc ce type de fatigue à l'EM/SFC spécifiquement, renforçant ainsi l’idée que cette fatigue soit unique, et très spécifique aux patients diagnostiqués EM/SFC. Les deux conditions seront vues comme étant des comorbidités, mais la fatigue invalidante, non soulagée par le repos, accompagnée de malaise post-effort, et où l’activité physique tend même à faire empirer les symptômes, sera la particularité même du diagnostic d’EM/SFC. Cette croyance est si bien ancrée dans l’esprit des patients, que j'ai déjà vu certaines personnes suggérer que le protocole d’effort cardiovasculaire sur 2 jours, développé par Staci Stevens et qui démontre objectivement que l’activité physique provoque une réponse physiologique anormale chez les personnes diagnostiquées d’EM/SFC, devrait pouvoir être utilisé pour confirmer le diagnostic d’EM/SFC. Or, je crains que cela puisse malheureusement venir porter préjudice au patient, dans un contexte où on pourrait se servir de ce test pour mettre un terme aux autres investigations médicales des causes pouvant venir expliquer - du moins en partie - la difficulté de récupération du patient. Pour ceux qui ne sont pas familiers avec ce protocole, en extrême résumé, on fait faire au patient 2 tests de VO2 Max à 24 heures d'intervalle. Chez une personne dite « normale », ou bien même souffrant de certains problèmes de santé chroniques, en théorie, leur capacité fonctionnelle (i.e. l'effort maximal qu'elle peut produire avant de risquer de souffrir d'un malaise cardiaque ou pulmonaire) devrait demeurer le même, ou bien même s'améliorer un peu du jour 1 au jour 2. Chez les patients diagnostiqués EM/SFC, si on leur demande de faire un effort qui dépasse le niveau de leur seuil anaérobie (i.e. le moment où le corps n'est plus capable d'utiliser efficacement l'oxygène pour produire son énergie, et se met à produire celle-ci par fermentation, créant plus de déchets, sous forme principalement d’acide lactique, qu'il arrive à en éliminer) alors leur capacité fonctionnelle diminue du jour 1 au jour 2. Ce que le protocole de Staci Stevens permet de faire, c’est de démontrer de façon objective la présence d’un trouble organique empêchant la personne diagnostiquée EM/SFC de récupérer normalement des suites d’un effort physique, et d’établir avec précision le seuil à partir duquel le patient n’arrive plus à produire son énergie en aérobie (et/ou bien que l’énergie produite en aérobie a déjà été entièrement consommée/ne peut plus être utilisée). Ce protocole a également permis de démontrer que virtuellement tous les patients diagnostiqués EM/SFC partagent cette particularité clinique. Mais sinon, à ma connaissance, il ne semble pas y avoir, à l’heure actuelle, d’études publiées démontrant objectivement que ce type de fatigue ne se retrouve pas chez d’autres sous-groupes de patients atteints de maladies chroniques immunitaires, inflammatoires, et/ou auto-immunes; puisque ces sous-groupes de « spoonies » ne semblent pas avoir été spécifiquement ciblés par ces études. Je sais que ce protocole a été évalué chez d'autres groupes de patients atteints de maladies chroniques, et qu'ils étaient capable de reproduire l'activité physique du jour 1 au jour 2 sans diminution significative de leur VO2 Max. Mais est-on spécifiquement allé chercher des patients de ces groupes qui résistent à l'approche conventionnelle, et ne semblent pas y mettre les mêmes efforts que les autres du point de vue de l'augmentation graduelle de leurs capacités? Ou bien avons-nous simplement pris des patients qui souffrent de ces diagnostics et qui se sont portés volontaires, possiblement parce qu'ils arrivent à récupérer de façon raisonnable suite à l'effort fournit? Du point de vue du SAMA, plus spécifiquement, il semble y avoir une théorie qui pourrait venir expliquer, du moins en partie, pourquoi l'individu est incapable d'offrir la même performance à ce test du jour 1 au jour 2. Tout d'abord, on sait déjà que l'activité physique est un pseudo-allergène pouvant déclencher une réaction pseudo-allergique chez les patients atteints de mastocytose systémique, de SAMA, ainsi que d’autres troubles de l’activation mastocytaire (comme, par exemple, l’anaphylaxie idiopathique). On sait aussi qu’il existe une autre condition de santé, encore inexpliquée, souvent associée aux troubles de l’activation mastocytaire, qui se nomme l’ « anaphylaxie induite par l'exercice ». L’anaphylaxie induite par l’exercice est un trouble où la personne qui fait de l'activité physique va tout à coup se mettre à présenter les même signes et symptômes qu'une réaction allergique de type anaphylactique, pouvant aller jusqu'à menacer sa survie. Or, on sait que les symptômes d'une réaction allergique ne se rendent pas toujours jusqu'au choc anaphylactique. Parmi ceux-ci, on peut retrouver des vertiges et étourdissements, des nausées, des malaises gastrointestinaux, des démangeaisons, de la fatigue, du brouillard cognitif, des bouffées de chaleur, de la transpiration abondante, de la congestion nasale, du larmoiement, etc. À l'époque où je n'étais pas encore sous traitements, je décrivais mon « malaise post-effort » comme étant une sensation d'être saoule ou intoxiquée. J'avais beaucoup de brouillard cognitif, d'étourdissements, de nausée, parfois des palpitations; occasionnellement, des sensations de fourmillements au niveau des extrémités (paresthésie), et simplement une sensation générale de malaise et de faiblesse. Parfois, je me sentais juste un peu affaiblie suite à l'effort, et c'est le lendemain, ou bien le surlendemain, que le plus gros des symptômes survenaient. Par la suite, je pouvais en avoir pour des jours, semaines, voire des mois à récupérer. La réaction pouvait donc se faire de façon soit immédiate, soit à retardement. Mais presqu'invariablement, une fois présente, elle tendait à s'entretenir dans le temps (en fonction de la demande en énergie initiale). Je me demande donc si le fameux malaise post-effort décrit par une certaine proportion de patients diagnostiqués EM/SFC, et qui semble également survenir chez un sous-groupe de patients atteints de SAMA (et possiblement d’autres maladies immunitaires ou auto-immunes), ne pourrait pas être une autre variante de l’anaphylaxie induite par l’exercice. Pour simplifier :
Chez un sous-groupe de personnes diagnostiquées EM/SFC, et/ou atteintes de SAMA, l’activité physique serait donc, plus ou moins, l’équivalent du gluten dans la maladie cœliaque. Si la personne atteinte de maladie cœliaque continue à être exposée au gluten, on va entretenir ses symptômes sans que son système ne puisse récupérer. Sa condition et son état général tend alors à s'agraver. Et, tout comme avec le gluten dans la maladie cœliaque; au début, il est possible qu’uniquement les activités de très forte intensité provoqueront des symptômes. Avec le temps et l’exposition régulière au pseudo-allergène, les patients deviennent de plus en plus sensibles à l’activité physique, ce qui fait en sorte qu’une activité aussi douce que de s’habiller peut finir par être suffisante pour déclencher la dégranulation mastocytaire. En encourageant le patient à graduellement augmenter les efforts malgré les symptômes, c'est finalement comme si on insistait pour l'exposer à nouveau au pseudo-allergène, alors que son organisme est déjà en train de gérer la crise pseudo-allergique précédente. Si on veut calmer la réaction pseudo-allergique et les symptômes, on doit alors chercher à minimiser l’exposition à l’élément déclencheur. Dans mon cas, le simple fait de me brosser les dents pouvait déclencher la dégranulation mastocytaire. Pour éviter les symptômes, ma marge de manœuvre était donc vraiment, mais alors là vraiment très mince. Serait-ce alors également possible qu’il existe certaines autres maladies immunitaires, ou auto-immunes chroniques, pouvant provoquer un syndrome d’activation mastocytaire secondaire, sans que toute la population de personnes atteintes par ces maladies n'en soit pour autant touchée? Ce qui expliquerait, peut-être, pourquoi l’activité physique serait si bénéfique pour aider certains patients à refaire leurs réserves d’énergie; alors que d’autres vivraient le phénomène opposé, et continueraient à s’épuiser plus on leur demanderait de s’activer physiquement? En théorie, l’activité physique est supposée avoir des propriétés anti-inflammatoires. Si elle est bien tolérée, il serait donc absolument logique qu’elle puisse aider à faire diminuer la douleur et la fatigue causées par l’inflammation dans plusieurs de ces maladies. Et qui dit moins d’inflammation, dit cellules du système immunitaire moins activées, dit moins grande demande de l’organisme en ATP, et dit soulagement de la fatigue. Les médecins qui croient que l’activité physique devrait soulager les symptômes inflammatoires et la fatigue de la fibromylagie, du lupus, et autres maladies inflammatoires on probablement parfaitement raison! Physiologiquement, c’est tout à fait ce qui devrait se passer. Mais voilà, chez les patients atteints de troubles de l’activation mastocytaire, on peut se retrouver avec le phénomène opposé, allant parfois jusqu’à l’anaphylaxie induite par l’exercice physique. De plus, comme je l'ai mentionné plus tôt, l’activation mastocytaire provoque la migration des mitochondries vers la surface des cellules, où elles se mettent alors à sécréter leur ATP (énergie cellulaire) et leur ADN à l'extérieur de celles-ci. L’ATP et l’ADN extracellulaires sont alors identifiés, à tort, comme des agents pathogènes par le système immunitaire, stimulant à nouveau l’activation mastocytaire, et entraînant un processus inflammatoire autocrine et paracrine. Fait intéressant, une étude aurait récemment démontrée que les mitochondries de certaines cellules immunitaires (soit les cellules mononuclées sanguines périphériques, i.e. les lymphocytes T, lymphocytes NK, lymphocytes B, et monocytes) des patients diagnostiqués EM/SFC produiraient TROP d'énergie cellulaire (ATP), et que la crête de leurs mitochondries serait légèrement plus condensée (ce qui indique probablement que la demande en production d'énergie est très forte, et que les mitochondries subissent donc beaucoup de stress pour fournir à la demande). Sinon, leur longueur, grosseur, forme, densité, le potentiel de leur membrane, leurs activités enzymatiques, et leurs complexes dans la chaîne de transport des électrons demeureraient intactes. Et, bien qu’il y aurait un surplus d’énergie produite par les cellules immunitaires au total, la quantité d’ATP produite par les mitochondries de ces cellules demeure tout à fait normale. Ce serait l’ATP provenant d'autres sources (produite par glycolyse ou anaérobie, par exemple), qui serait présente en quantités impressionnantes (plus du double d’une personne normale)! Donc, si on se fie aux résultats de cette étude, il semblerait que la fatigue chez les patients diagnostiqués EM/SFC ne serait pas causée par une dysfonction des mitochondries cellulaires elles-mêmes. En théorie, elles produisent la même quantité d’ATP qu’une personne en bonne santé. Par contre, cela suggère qu’il y a peut-être « quelque chose » dans l’environnement extracellulaire (ex : plasma sanguin) qui ferait en sorte que presque toute l’ATP mitochondriale disponible soit consommée pendant que le patient est au repos, avant même que la personne tente d’effectuer un effort (et fasse ainsi augmenter la demande en ATP globale de l’organisme). Une des théories de Dr. Wang serait donc que les cellules du système immunitaire étudiées (lymphocytes T, B, NK, etc.) étaient en état d’activation; possiblement à cause d’une infection virale ou bien d’une autre condition. Et que, lorsque activées, ces cellules tendent à passer du catabolisme (réactions chimiques de synthèse moléculaire) à l'anabolisme (réactions chimiques de dégradation moléculaire). La demande en énergie (ATP) augmente donc, et elles deviennent de plus en plus dépendantes de la glycolyse pour pouvoir subvenir à leurs besoins. Ce qui expliquerait pourquoi elles produiraient plus du double d’ATP par glycolyse ou anaérobie qu’on retrouverait chez une personne normale, et que la demande en énergie cellulaire serait si massive chez une personne diagnostiquées EM/SFC. Or, comme on l’a vu plus haut, les cellules mononuclées sanguines périphériques possèdent toutes des récepteurs de l’histamine, et leur activité est également modulée par les mastocytes via les médiateurs chimiques (cytokines, chimiokines, TNFα, etc.) qui sont relâchés, entre autres, lors de la dégranulation mastocytaire. Donc, la réponse à l’activité physique d’une personne atteinte de SAMA (pour laquelle l’activité physique est un pseudo-allergène), serait peut-être la suivante :
Pendant tout ce processus, l’organisme de la personne atteinte de SAMA aura donc besoin de quantités massives d’ATP pour subvenir à ses besoins, soit :
On sait aussi qu’une réaction allergique prend généralement de 24 à 48 heures à se résorber. Et, on peut probablement supposer que, si l’effort demandé à l’organisme est maximal, peu importe le niveau d’intensité normalement requis pour déclencher la dégranulation mastocytaire chez un patient dont l’activité physique fait partie des facteurs déclencheurs, la réaction pseudo-allergique risque inévitablement de se produire. Donc, si cette même personne atteinte de SAMA effectue 2 tests d’endurance cardiovasculaires à 24 heures d’intervalles, nous pourrions probablement observer le phénomène suivant :
Du jour 1 au jour 2, on peut donc assumer que le seuil anaérobique sera atteint plus rapidement, et que l’effort maximal pouvant être fourni sera plus bas, puisque les réserves en ATP normalement disponibles n’auront pas eu le temps de bien se renouveler, et/ou que le processus inflammatoire (soit encore actif, et/ou qu’on vient de restimuler en exposant à nouveau l’organisme à un facteur déclencheur de dégranulation mastocytaire) fera compétition à l’effort physique qu’on lui demande de fournir au niveau des besoin de consommation en ATP pendant le test. Par le repos, on diminue la demande en ATP de l’organisme, et on évite d’activer les mastocytes d’avantage en les exposant à un pseudo-allergène, i.e. l’activité physique. Ce qui, éventuellement, va donner une chance au patient de graduellement sortir de son « crash » énergétique. D’où la grande importance d’apprendre à la personne atteinte de SAMA à respecter son « seuil d’activation mastocytaire » lors de toute activité physique, et de porter une grande attention à ses malaises et ses symptômes le jour même, ainsi que dans les jours qui suivent. Tandis que, si on tente de lui imposer un programme d’exercices gradués qui, éventuellement, lui font franchir ce seuil de tolérance, non seulement on continue à entretenir le processus inflammatoire pseudo-allergique systémique par l’exposition constante à un pseudo-allergène. Mais on maintient une demande en ATP de plus en plus élevée, alors que les capacités de production d’ATP de l’organisme sont déjà sollicitées au maximum. Tout cela, c’est sans compter les nombreux symptômes pouvant découler du déversement de l’histamine, héparine, sérotonine, et autres médiateurs lors de la dégranulation mastocytaire dans l’organisme, qui vont aller stimuler les récepteurs situés sur d’autres organes. Et, c’est sans compter tous les autres pseudo-allergènes potentiels du SAMA (tels que les émotions, les changements de température, l’exposition à la lumière du soleil, le contact avec l’eau, les odeurs, les sons, les vibrations d’une voiture, etc.), auxquels la personne atteinte pourrait être exposée au courant de la même période. Donc, même si la personne atteinte de SAMA cesse de bouger et s’impose un repos strict, il est absolument possible qu’elle continue quand même à consommer de grandes réserves d’ATP au quotidien, parce que ses mastocytes s’activent et dégranulent en quasi-permanence. Si elle arrive à identifier virtuellement tous ses facteurs déclencheurs et à les éviter, elle va probablement pouvoir maintenir ses symptômes sous contrôle. Mais, si ceux-ci sont trop multiples, varient, incluent l’effort physique, et ne peuvent être évités; à moins d’avoir accès à des traitements appropriés, le déficit énergétique risque d’être très profond, et ses systèmes de production d’énergie vont probablement fonctionner à toute allure jour et nuit. Est-ce que cette théorie s'appliquerait à tous les patients atteints d'EM/SFC? Probablement pas. J'ai déjà eu la chance de m'entretenir brièvement avec des chercheurs qui étudient présentement les troubles de production d'énergie dans l'EM/SFC, dont le Dr. Ron Davis, et il semble que la piste d'un trouble de l'activation mastocytaire n'expliquerait pas le phénomène qui se produit dans le cas de patients très sévèrement atteints d'EM comme celui son fils. Dans mon cas à moi, ce qu'on sait pour sûr, c'est qu'avant mes traitements actuels, ma réaction adverse à l'activité physique était typique des patients diagnostiqués EM/SFC. En effet, en novembre 2012, je suis allée au « Department of Exercise and Sports Sciences » du Collège d'Ithaca (dans l'État de New York) pour y rencontrer Dr. Betsy Keller (une chercheuse qui se spécialise, entre autres, au niveau de l'impact de l'activité physique chez les patients diagnostiqués d'EM/SFC, et qui utilise le protocole développé par Staci Stevens dans ses recherches), pour y effectuer le test d'endurance cardiovasculaire sur 2 jours. Le premier jour, j'avais une capacité maximale (VO2 Max) de 6.2 METS. Le deuxième jour, cette valeur a chuté à 5.7 METS. Puisque, pendant toute la durée de l’exercice, on mesure en tout temps les échanges gazeux et la fréquence cardiaque, ainsi que la pression artérielle à intervalles réguliers, on peut facilement se prononcer sur le fait que l'effort fournit par le patient était maximal ou non. Celui-ci ne peut pas fausser les résultats en choisissant d'en faire « un peu moins » le lendemain. Cela se verrait tout de suite. Mon seuil anaérobie lors des tests était de 2.1 METS (avec une légère diminution de sa valeur en ml/kg/min le 2ème jour). Et, selon l'échelle utilisée à l'époque*, s'habiller correspondrait à 2.5 METS. *Note : Les valeurs ont été réajustées depuis 2012, autant point de vue des résultats obtenus, que des valeurs estimées pour chaque tâche. Donc, juste le fait de m'habiller pouvait me faire tomber en anaérobie. C'est bas. Ridiculement bas. Pour éviter d'empirer mes symptômes, Dr. Keller me recommandait donc d'éviter de dépasser ce seuil (qui équivalait également à 112 battements par minute au niveau de la fréquence cardiaque) pendant 95% à 99% de ma journée, sinon j'entretenais ceux-ci, et n'arrivais pas à récupérer. Ces résultats sont tout à fait typiques de ce que l'on retrouve chez un patient diagnostiqué EM/SFC. C'est le même type de réponse aberrante et anormale à l'activité physique dont souffre tous ces patients. Alors que, chez un patient atteint de SAMA, la réaction adverse à l’activité, lorsque présente, est tout simplement considérée comme résultant de la dégranulation mastocytaire. On recommande donc aux patients qui en sont atteints de continuer à s'activer uniquement à l'intérieur de leur propre seuil de tolérance, pour éviter de déclencher les symptômes. Ce seuil de tolérance est unique à chaque individu, et peut varier en fonction de la réponse positive aux traitements. Par contre, il ne semble pas que les chercheurs se soient intéressés tout particulièrement à ce qui cause spécifiquement la fatigue ressentie par les patients, et/ou l’impact que la dégranulation mastocytaire pourrait avoir sur la production et/ou bien l’utilisation d’ATP lors de l’activité physique. Un peu comme s’il était tellement logique qu’une personne dont l’organisme est bombardé d’histamine, sérotonine, héparine, et de tout plein d’autres médiateurs modulant la réponse inflammatoire soit fatiguée, que le plus important est de trouver des solutions pour tenter de stabiliser les mastocytes, et faire diminuer l’inflammation. Donc, la seule chose sur laquelle je peux me fier pour savoir si ma réponse à l’activité physique est « typique » des patients atteints de SAMA pour lesquels l’exercice peut déclencher les crises, ce sont les témoignages de patients et d’associations de patients . À cet effet, j’ai trouvé cet extrait d’une lettre qui a été publiée en janvier 2011 (et mise à jour en avril 2012), par la Société canadienne de la mastocytose : « La mastocytose, le SAMA, et l’AI (anaphylaxie idiopathique) ont un impact négatif sur la vie personnelle et professionnelle des patients. Plusieurs peuvent avoir une diète restreinte de seulement quelques aliments qu’ils peuvent consommer de façon sécuritaire, souffrent de fatigue de façon constante, d’épisodes de vertige et d’anaphylaxie, en plus d’une incapacité à faire de l’exercice (incluant la marche) de façon régulière à cause de leur fatigue, faiblesse musculaire, et tous les autres symptômes. À la lecture de cette lettre, décrivant l’expérience vécue au quotidien par les patients atteints de SAMA, il semblerait donc que oui, le type de fatigue que j’éprouvais semble assez « typique » de la fatigue ressentie par une personne atteinte de SAMA, et on peut probablement supposer que, si c’est patients effectuaient un test d’endurance cardiovasculaire sur 2 jours, ils obtiendraient probablement des résultats similaires.
Donc, une fois que la physiopathologie du SAMA semble fournir une explication plutôt solide derrière mon intolérance à l'effort, et mes « crash » énergétiques. Qu'est-ce qui me resterait comme symptômes appartenant exclusivement à l'EM/SFC? Tous les symptômes de l'EM/SFC semblent se retrouvert aussi dans la liste de symptômes possibles du SAMA, incluant une fatigue qui ne dépend ni de l'effort physique fournit, ni d'une mauvaise qualité du sommeil, mais bien d'une réaction adverse pseudo-allergique à l'effort. Par contre, dans le SAMA, la présence d'une telle fatigue chez le patient n'est pas un critère diagnostic essentiel pour la pose du diagnostic. Oui, la fatigue est la plainte la plus fréquente, et très invalidante. Par contre, ce n'est pas tous les patients qui sont atteints de SAMA qui présentent ce type particulier de fatigue. Rappelons que le SAMA a le potentiel d'affecter tous les organes et tous les systèmes du corps, mais que ceux-ci ne sont pas nécessairement tous atteints, ni de la même façon, ou bien avec le même niveau de sévérité. Et ils n’ont pas non plus les mêmes facteurs déclencheurs! Peut-être que chez certains patients atteints de SAMA, le processus derrière l’activité physique fonctionne normalement, et la personne atteinte bénéficie donc de l’action anti-inflammatoire de l’exercice sur son organisme. La fatigue serait moindre, et déclenchée par des odeurs ou l’exposition à des produits chimiques, par exemple. Aller prendre une bonne marche dans une aire ventilée l’aiderait à se sentir mieux. Je ne fais pas d'anaphylaxie, j'ai vraiment très peu de réactions cutanées (et celles-ci tendent à être très transitoires... Ex: plaques rouges sur la poitrine au contact de l’eau tiède ou chaude qui ne provoquent aucune douleur ni démangeaison, puis disparaissent dans l'heure qui suit mon bain ou ma douche), je n'ai pas de bouffées de chaleur où mon visage devient tout rouge. Par contre, lorsque particulièrement fatiguée, je vais avoir l'impression de faire de la fièvre, et la température de mon visage devient très chaude au toucher (malgré un teint globalement normal). Certains des symptômes les plus « typiques » du SAMA sont absents chez moi. Mon problème principal était vraiment au niveau de la fatigue, de l'intolérance à l'effort, et du temps de récupération anormalement long suite à celui-ci. L’autre différence, c’est simplement que le diagnostic de SAMA ne peut être donné en se basant uniquement sur l’observation et la documentation des symptômes du patient en l’absence de tout autre diagnostic pouvant venir expliquer leurs symptômes. Bien que le SAMA demeure un diagnostic d’exclusion, on doit quand même pouvoir objectiver l’activation mastocytaire en démontrant un surplus de médiateurs produits par les mastocytes dans l’organisme. Les définitions plus globales de l'EM/SFC, quant à elle, mettent vraiment l'emphase tout particulièrement sur la fatigue et le malaise post-effort, mais le patients n'a pas besoin de démontrer de signes d'activation mastocytaire abberrante pour recevoir le diagnostic. Si on regarde d'autres points que l’EM/SFC et le SAMA semblent avoir en commun, il pourrait être bon de souligner qu'on retrouve régulièrement le SAMA chez les personnes atteintes du syndrome de tachycardie orthostatique posturale (STOP), et/ou du syndrome d’Ehlers-Danlos (SED). Il est d'ailleurs possible que ces trois syndromes partagent une mutation génétique commune, et on parle souvent de ceux-ci comme appartenant à un seul et même groupe de maladies connexes. La fibromyalgie et le syndrome de l’intestin/côlon irritable sont aussi des diagnostics souvent préexistants chez les personnes qui reçoivent le diagnostic du SAMA. De plus, une étude a déjà démontré que la bactérie responsable de la maladie de Lyme (Borrelia burgdorferi) pourrait induire l'activation mastocytaire, et la libération de cytokines par ceux-ci. J’ai également vu quelques témoignages de patients atteints de la maladie de Lyme dont les symptômes se seraient améliorés suite à l’introduction de médicaments stabilisateurs des mastocytes (ex : Kétotifen) dans le régime thérapeutique. Le Dr. Daniel Jaller semble rapporter des observations similaires. La maladie de Lyme est également un diagnostic très associé à l'EM/SFC. Plusieurs patients diagnostiqués EM/SFC sont d’ailleurs convaincus d’avoir la maladie de Lyme, malgré des résultats de tests négatifs. Je ne dis pas que l'encéphalomyélite myalgique et le syndrome d'activation mastocytaire sont la même chose. Au contraire. En ce qui concerne l’encéphalomyélite myalgique, je suis plutôt convaincue que Dr. Hyde ait raison, et qu’il existe à tout le moins une cohorte spécifique atteinte d'une forme de poliomyélite. Ainsi que possiblement d'autres cohortes (ex: COVID long) qui risquent de se définir de plus en plus au courant des prochaines années. Par contre, je me demande également si certaines infections virales, également responsables de l'EM, pourraient potentiellement déclencher un syndrome d’activation mastocytaire (secondaire) chez un patient qui en est atteint. Et si cette activation mastocytaire anormale pourrait donc aussi être impliquée dans le mécanisme physiopathologique responsable de l'intolérance à l'activité physique avec malaise post-effort, avec temps de récupération anormalement long (entre autres), chez certains de ces patients souffrant d'encéphalomyélite myalgique. En fait, je me pose la question si, en quelque part, le SAMA ne pourrait pas venir expliquer pourquoi certains patients atteints de ces deux maladies infectieuses (maladie de Lyme et encéphalomyélite myalgique), et peut-être plusieurs autres sortes de maladies infectieuses différentes, arrivent à se rétablir suite à la phase initiale et/ou même secondaire de l’infection; alors que d'autres vont développer la forme chronique de ces maladies. En partant de l’hypothèse que les troubles de l’activation mastocytaire pourraient être liés à une ou plusieurs mutations génétiques (qui possiblement affecteraient aussi les patients atteints de STOP, et du syndrome d’Ehlers-Danlos), alors serait-il possible qu’il existe des gens qui seraient tout simplement plus susceptibles de développer des troubles de l’activation mastocytaire suite à certains éléments déclencheurs (vaccins, infections, grossesse, période de haut stress, exposition à des produits chimiques, etc.) que d’autres? Par contre, je tiens vraiment à préciser que la présence d’un trouble de l’activation mastocytaire chez ces patients n’invaliderait absolument en rien ces autres diagnostics primaires, ni le fait que le SAMA (secondaire) puisse être associé à de nombreuses maladies entièrement distinctes et différentes les unes des autres. La maladie de Lyme est une infection causée par une bactérie. L’encéphalomyélite myalgique est une infection causée (fort probablement) par un entérorivus. Ce sont deux maladies différentes, avec deux causes différentes, mais des symptômes similaires (impliquant peut-être, ou non, une activation mastocytaire chronique). Dans le cas d’un virus, la forme de traitement la plus efficace demeure la prévention de l’infection via l’immunisation. Sinon, une fois la personne infectée, on peut probablement réduire la sévérité et l'impact de la maladie chez la personne atteinte grâce à des traitements antiviraux, surtout si la présence du virus est détectée rapidement. Les maladies infectieuses nécessitent une prise en charge thérapeutique rapide pour éviter d’en subir les conséquences à long terme. Certains dommages permanents au niveau des nerfs, entre autres, peuvent survenir. Il ne faudrait donc surtout pas que le SAMA, en particulier sous sa forme idiopathique, devienne un diagnostic « poubelle » (ce qui est malheureusement un peu le cas avec l'EM/SFC en ce moment) pour venir expliquer toute maladie étrange à laquelle le médecin ne trouve pas d'explication. En effet, les symptômes du SAMA peuvent imiter un nombre important d'autres maladies, sont hétérogènes, et ne sont nullement spécifiques au SAMA non plus. Cela veut donc dire que le risque de passer à côté d'un autre diagnostic en se basant uniquement sur les symptômes, ou bien même la présence d'un surplus d'histamine dans l'organisme grâce aux tests de laboratoire, est vraiment très grand. Par contre, une fois que le patient a été bien investigué à fond, que toutes les causes traitables derrière ses symptômes ont été prises en charge, et/ou qu’on n’arrive tout simplement pas à trouver d’autre explication derrière les symptômes, cela donne définitivement espoir qu'il puisse y avoir des pistes de traitement possibles à explorer pour soulager ces patients de façon palliative. L'idéal est toujours d'agir directement sur la cause. Mais, si la cause n'est pas réversible ou bien impossible à trouver, alors on n'a d'autre choix que de se rabattre sur le traitement des symptômes. À moins d'être primaire, et/ou bien le fruit d’une mutation génétique innée ou acquise, le SAMA est fort probablement la conséquence d’un autre problème de santé qui agit sur les mastocytes, et non la cause directe de l’activation mastocytaire. Par contre, ces mastocytes déréglés par « quelque chose » ont le pouvoir d’aller, à leur tour, dérégler l’ensemble de tous les systèmes corporels! Si on ne trouve pas un moyen de les stabiliser, ou bien de les empêcher d’envoyer des signaux anormaux aux autres cellules du système immunitaire et organes corporels, alors rien ne va plus! En ce moment, j'ai donc un diagnostic de SAMA idiopathique, puisque mon SAMA ne semble pas être secondaire à une autre condition identifiable (et il est encore trop tôt pour parler de mutation génétique). Pendant longtemps, j'ai cru que ma mononucléose infectieuse (que j'avais contractée en 2006) avait été le facteur déclencheur, mais il semble que certains signes et symptômes étaient déjà présents à l'époque où j'avais fait mon zona (en 2004), et même dans l'enfance (TDAH, asthme et pneumonies à répétition, hyperlaxité des articulations, troubles d'intégration sensorielle, troubles d'acquisition de la coordination au niveau de la motricité globale...) et à l'adolescence (eczéma, apparition de quelques nouvelles allergies et sensibilités environnementales qui n’étaient pas présentes dans l’enfance...). En fait, tout ce que je sais pour sûr, c'est que de juin 2009 à avril 2016, avant que mes injections d'Omalizumab (Xolair) commencent à faire effet (ce qui a pris 3-4 mois environ), j'étais principalement confinée à domicile, avais besoin d'un fauteuil roulant poussé par une autre personne pour circuler à l'hôpital lors de mes rendez-vous médicaux (ou bien les rares fois dans l’année où j’arrivais à tolérer une sortie au cinéma); étais incapable de préparer mes propres repas, m'habiller à tous les jours, ou bien vivre seule; et je pouvais en avoir pour quelques jours à me remettre d’un dîner ou bien d’un souper occasionnel au restaurant. Maintenant [août 2017], certains symptômes neurocognitifs (plutôt significatifs et envahissants) et un certain niveau de fatigue persistent. Par contre, je peux maintenant marcher 20 km (total) dans une seule journée, faire du ski alpin pendant près de 4 heures consécutives, faire 1 heure de pratique de danse par jour de semaine... Le tout, sans déclencher de malaise post-effort, ni en avoir pendant des jours à m’en remettre. Oui, il m’arrive occasionnellement de dépasser un peu mes limites et d’être plus fatiguée le jour même ou bien le lendemain. Par contre, je n’ai plus à « payer pour » pendant des semaines. Une ou deux journées à me tenir plus tranquille, et je reviens à mon niveau de fonctionnement antérieur (par rapport au point où j’en suis rendue au niveau de la récupération de mes capacités fonctionnelles depuis le début des traitements, et non mon niveau de fonctionnement antérieur au SAMA). Sinon, je constate en effet que je suis toujours un peu moins en forme que d’autres personnes de mon âge. Par exemple, ma fréquence cardiaque peut facilement monter entre 160 et 185 battements par minute pendant mes cours de danse, et je dois occasionnellement prendre des pauses à cause de la fatigue musculaire, alors que les autres élèves (dont certains plus âgés que moi) semblent n’avoir aucun problème à maintenir le rythme. Ma peau rougit plus vite pendant l’effort, et je transpire de façon beaucoup plus abondante qu’avant la maladie. Mais encore là, l’intensité de l’activité ne va pas déclencher de malaise post-effort, ni vider toutes mes réserves d’énergie pour le reste de la journée, et surtout les jours suivants. J’arrive à regénérer celles-ci à un rythme beaucoup plus raisonnable. Donc, pour moi, ces améliorations semblent vraiment suggérer qu'il y a une forte possibilité que les mastocytes puissent être responsables (du moins, en partie) du processus inflammatoire chronique qui provoque le malaise post-effort, et entretient l’épuisement énergétique suite à celui-ci. Et je peux très bien imaginer la possiblité qu'il existe un certain sous-groupe de patients, qui n'ont jamais été investigués pour le SAMA, et qui vivent aujourd'hui avec un diagnostic d'EM/SFC, de lupus, de maladie de Lyme, de syndrome d'Ehlers-Danlos, de STOP, et/ou bien d'autres maladies similaires, dont le processus pathologique derrière le maintien de la fatigue pourrait être similaire. Et surtout, ces améliorations démontrent qu'en tentant de stabiliser l'activation mastocytaire, et/ou bien de bloquer les médiateurs chimiques libérés par les mastocytes grâce à des traitements appropriés, on peut possiblement aller chercher un certain soulagement de la fatigue chez ces patients, et améliorer leur qualité de vie. Il est, bien sûr, très possible que mon interprétation de l'article de Dr. Theoharides concernant la façon dont les mastocytes agissent sur les mitochondries et les cellules du système immunitaire soit erronée; et/ou que ma théorie sur l’explication de la présence d’un surplus d’énergie produite par glycolyse ou anaérobie au niveau des cellules du système immunitaire des patients atteints de SAMA ne tienne pas du tout. Néanmoins, je demeure convaincue qu’un très quand nombre de personnes qui, aujourd’hui, vivent avec le diagnostic d’EM/SFC, en particulier celles qui, parmi leurs symptômes et conditions associées, ont : - des réactions cutanée, - des bouffées de chaleur, - de l’hypersensibilité chimique multiple, - des intolérances alimentaires et/ou environnementales (dont certaines ou même plusieurs sont apparues après le début de la maladie), - la maladie coeliaque, le syndrome de l’intestin/côlon irritable, de la dysmotilité ou du reflux gastrique, et/ou autre atteintes gastro-intestinales, - du brouillard cognitif, - l’autisme ou le TDAH, - des troubles et/ou ou antécédents de troubles atopiques (eczéma, asthme, rhinites allergiques…), - de la difficulté à avaler, et/ou un diagnostic d’œsophagite à éosinophiles (un autre problème de santé hautement associé aux troubles de l’activation mastocytaire), - de la dysautonomie ou le STOP, - le syndrome d’Ehlers-Danlos, et/ou autres maladies des tissus conjonctifs, - de la cystite interstitielle, vulvodynie, et/ou prostatite, - de la difficulté à moduler leur température interne, remplissent probablement les critères diagnostics pour le SAMA. Sinon, je ne crois en effet pas que le « syndrome de fatigue chronique » existe comme entité clinique distincte en tant que tel. Je pense vraiment que, parmi les patients actuellement diagnostiqués EM/SFC au Canada, on retrouve : - un sous-groupe atteint d’encéphalomyélite myalgique d'origine entérovirale, - un sous-groupe atteint d'encéphalomyélite malgique suite à un épisode ou plusieurs épisodes infectieux d'autres origines, - un sous-groupe souffre d’autres pathologies non identifiées, et souvent traitables (ce qui inclue toute la panoplie de maladies rares et orphelines), - un sous-groupe souffre possiblement de mastocytose systémique, ou de syndrome d’activation mastocytaire monoclonal, - un sous-groupe souffre possiblement d’un syndrome d’activation mastocytaire idiopathique, i.e. dont on ne connait pas encore l’origine, et - possiblement d'autres sous-groupes, dont les symptômes peuvent être liés à tout plein d'autres facteurs qu'on a encore beaucoup de difficulté à s'expliquer. Et il existe peut-être plusieurs autres sous-groupes à travers le sous-groupe de SAMA idiopathique, qui seront appelés à émerger au fur et à mesure qu’on arrivera à mieux comprendre et expliquer les différentes causes possibles du SAMA. Sources et références
4 Commentaires
Kahn
30/1/2018 15:18:11
Bonsoir,
Répondre
Jean-Francois Nandancee
23/12/2022 14:03:13
Docteur lucie wetchoko
Répondre
Aurélie
16/5/2018 04:12:59
Bonjour,
Répondre
Mae
3/7/2020 05:45:07
Bonjour,
Répondre
Laisser un réponse. |

 Flux RSS
Flux RSS
